
- Симптоматические проявления
- Факторы, способствующие возникновению заболевания
- Диагностические методы
- Лечение
- Прогноз выживаемости
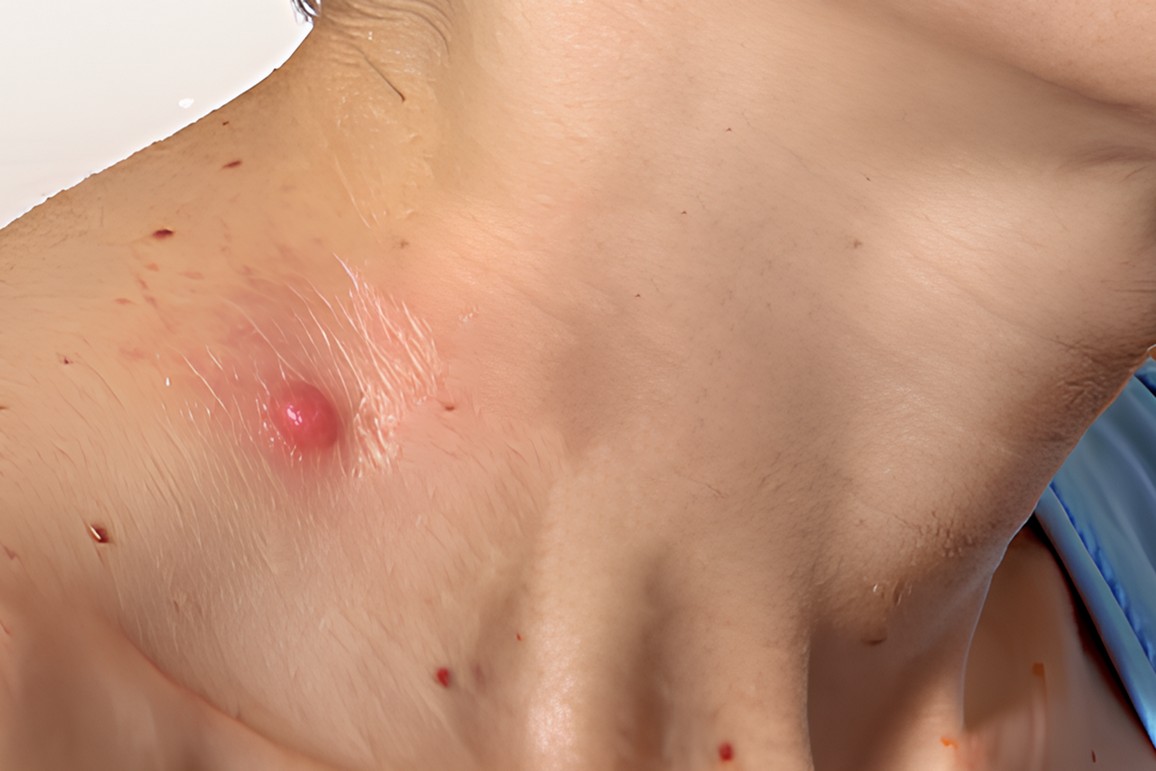
Дерматофибросаркома – опухолевый очаг, который медленно растет и, развиваясь, поражает близрасположенные ткани. Местом расположения опухоли являются лицо, ягодицы, паховые зоны, тело. С последним случаем врачи сталкиваются чаще. Цвет новообразования зависит от стадии патологии: он может быть красным и темно-коричневым.
Симптоматические проявления
Клинические признаки глиосаркомы тесно связаны с местоположением новообразования и, как правило, развиваются постепенно. На ранней стадии, когда клетки организма подвергаются мутациям и активно делятся, какие-либо внешние проявления отсутствуют. В дальнейшем на коже могут возникать узелки, а цвет новообразования изменяется, приобретая бордовый оттенок, что часто не привлекает особого внимания.
Спустя несколько месяцев в области поражения наблюдается отечность, а само новообразование становится округлым и достигает размера от 2 мм. Оно может быть как одиночным, так и формировать группы, соединенные мягкими тканями. Постепенно опухоль становится более выраженной, выступая над поверхностью кожи. Если не проводить терапию, примерно через шесть месяцев на поверхности новообразования формируются кровоточащие свищи или язвы. На этом этапе возникает болевой синдром в пораженной области.
Опухоль приобретает красновато-фиолетовый цвет, становится гладкой и блестящей, на ней хорошо видны многочисленные кровеносные сосуды, язвы, эрозии и свищи. Размер новообразования может варьироваться от 2 до 6 сантиметров. Медленное развитие заболевания и метастазирование могут длиться до двух десятков лет.
Атипичные клетки способны распространяться в лимфатические узлы, мышцы, кости, внутренние органы и даже головной мозг. Важно отметить, что рецидивы возникают более чем в половине случаев данного заболевания. Своевременная диагностика и адекватное лечение играют решающую роль в предотвращении распространения опухоли и улучшении прогноза для пациента.
Факторы, способствующие возникновению заболевания
Несмотря на то, что точные механизмы развития дерматофибромы до сих пор остаются предметом активных исследований, ученые выявили ряд факторов, значительно повышающих вероятность появления этого новообразования. Эти факторы риска, выявленные на основе статистических данных и клинических наблюдений, позволяют определить группы населения, наиболее уязвимые к данному заболеванию.
Одним из ключевых аспектов является генетическая предрасположенность. Наличие дерматофибромы у близких родственников может указывать на повышенную вероятность ее развития у индивида, независимо от его возраста или пола. Хотя конкретные гены, ответственные за эту предрасположенность, еще не идентифицированы, семейный анамнез является важным диагностическим признаком.
Влияние окружающей среды также играет существенную роль. Воздействие неблагоприятных экологических факторов, токсичных химических веществ и ионизирующего излучения может повредить клетки кожи и спровоцировать развитие дерматофибромы. Проживание в экологически неблагополучных районах или работа на вредных производствах увеличивает риск заболевания.
Статистические данные указывают на то, что женщины более подвержены дерматофиброме, чем мужчины. Эта разница может быть связана с гормональными особенностями женского организма или с различиями в образе жизни и профессиональной деятельности. Кроме того, возраст является значимым фактором риска, поскольку большинство случаев дерматофибромы диагностируется у людей в возрасте от 40 до 60 лет.
Нельзя недооценивать роль травматических повреждений кожи. Даже незначительные травмы, такие как ушибы, порезы, укусы насекомых или мозоли, могут стать отправной точкой для развития дерматофибромы. Воспалительные процессы и нарушения регенерации тканей, возникающие в результате травм, могут способствовать образованию новообразования. Наличие определенных заболеваний, таких как туберкулез, оспа, гепатит и другие, может повысить восприимчивость организма к дерматофиброме, вероятно, из-за ослабления иммунной системы и нарушения ее регуляторных механизмов.
Диагностические методы
Первичная диагностика начинается с визуального осмотра новообразования врачом, в ходе которого оцениваются его характеристики и особенности проявления заболевания. Для подтверждения предварительного диагноза и определения типа опухоли проводится биопсия с последующим гистологическим анализом полученного образца в лабораторных условиях. Биопсия может быть выполнена методом тонкоигольной аспирации или открытым хирургическим доступом. Нередко, биопсия проводится уже после оперативного удаления опухоли.
Для определения наличия метастазов и оценки степени распространения опухолевого процесса применяются различные методы диагностической визуализации, включая: ультразвуковое исследование лимфатических узлов, компьютерную томографию органов брюшной полости, рентгенографию костей, расположенных в непосредственной близости к очагу поражения, а также рентгенографию органов грудной клетки.
Современные методы диагностики, такие как ПЭТ-КТ и МРТ с контрастированием, позволяют визуализировать самые мелкие метастазы и получать максимально точную информацию о распространении опухоли. Это дает возможность врачам принимать обоснованные решения о тактике лечения, будь то хирургическое вмешательство, лучевая терапия, химиотерапия или их комбинация.
 Источник фото https://ru.freepik.com/, автор @freepik
Источник фото https://ru.freepik.com/, автор @freepik
Лечение
Наиболее эффективным методом лечения глиосаркомы является хирургическое удаление опухоли с захватом окружающих тканей (не менее 5 см), однако при неполном удалении возможны рецидивы, которые могут быть более агрессивными. Операция Моса, выполняемая под микроскопом с поэтапным удалением раковых клеток и мгновенной заморозкой тканей, практически исключает рецидивы, но ограничена в применении из-за высокой стоимости и недоступности. Химиотерапия, используемая как часть комплексного лечения, позволяет остановить рост опухоли, уменьшить ее размеры и предотвратить метастазирование, способствуя стойкой ремиссии. Радиационная терапия, основанная на воздействии ионизирующего излучения на раковые клетки, замедляет развитие ракового процесса и повышает шансы на успех хирургической операции, а также используется для профилактики рецидивов; в случаях, когда хирургическое вмешательство невозможно, она может применяться как основной метод лечения, хотя и с меньшей эффективностью. Несвоевременная диагностика, неправильное лечение, рецидивы и распространение атипичных клеток могут привести к поражению соседних тканей и внутренних органов, а также к развитию лейкоза и меланомы; негативные эффекты могут возникать и в процессе или после применения различных методов лечения.
Прогноз выживаемости
Обнаружение первичных или вторичных отдаленных метастазов, проникших глубоко в ткани, существенно ухудшает прогноз. В таких ситуациях ожидаемая продолжительность жизни, как правило, не превышает одного-двух лет. Несмотря на это, стоит отметить, что отдаленные метастазы, к счастью, формируются сравнительно редко – лишь в 5-7% случаев данного заболевания.
Современная онкология располагает широким спектром методов, направленных на продление жизни пациентов с метастатическими формами заболевания. Химиотерапия, таргетная терапия, иммунотерапия и лучевая терапия могут применяться как по отдельности, так и в комбинации, позволяя достичь контроля над ростом опухоли и улучшить качество жизни пациента.
При выборе тактики лечения учитывается множество факторов, включая общее состояние пациента, локализацию и размер метастазов, наличие сопутствующих заболеваний и индивидуальную чувствительность к различным препаратам. Важным аспектом является также психологическая поддержка пациента и его близких, поскольку борьба с онкологическим заболеванием требует значительных усилий и стойкости.
Несмотря на серьезность прогноза при обнаружении отдаленных метастазов, не стоит терять надежду. Постоянное развитие онкологии, появление новых методов лечения и возможность индивидуального подхода к каждому пациенту позволяют надеяться на улучшение результатов лечения и повышение выживаемости даже в самых сложных случаях.